近年來,隨著基因組學的進步,針對病患個人狀況量身規劃的精準醫療,成為醫學發展的新趨勢。
多方數據顯示該產業正蓬勃發展。根據臺灣國發會的調查,臺灣再生醫學與精準醫學等精準健康領域每年營收約 632 億元。全球方面,根據市調公司 Frost & Sullivan 的資料,預估 2025 年精準醫療市場規模將達到 3.7 兆新臺幣。
替身醫療:實現精準醫療的新方式
本文想探討的「替身醫療」正是實現精準醫療的一種方式。「替身醫療」一詞最初由精拓生技提出,雖然不是嚴格定義的醫學術語,但作為一種概念框架,它的核心理念是:在病患實際接受治療方案前,透過虛擬或實體的「替身」進行模擬測試,以優化藥物篩選和制定治療方案。
替身醫療的三大實踐方向
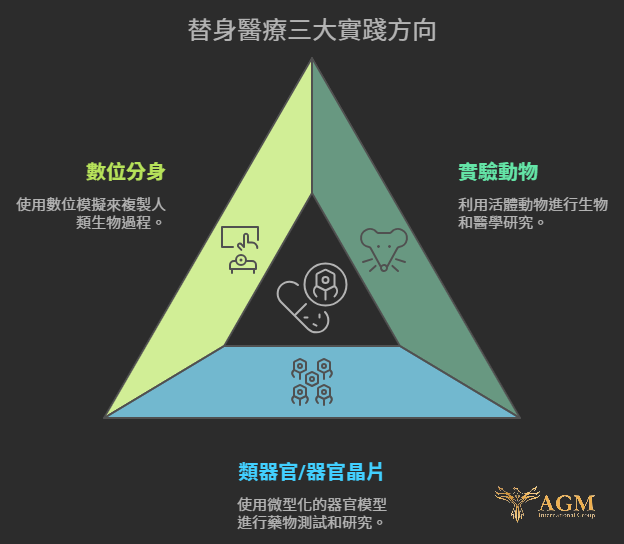
觀察市面上現行的技術,替身醫療的實踐大致可歸納為以下三大方向:實驗動物、類器官/器官晶片 ( Organoids/Organ-on-a-chip )、以及數位分身 ( Digital Twins ) 。
實驗動物
在替身醫療的三個方向中,技術歷史最悠久、現階段應用最普及的,當屬實驗動物。實驗動物的應用起源於西方醫學,早期的解剖學與生理學研究即大量依賴動物實驗。到了 19 世紀,隨著達爾文和波納的研究推動,動物模式開始替代人類模式,成為醫學研究的重要基礎,實驗動物的使用也因此大幅增加。
直至今日,動物實驗仍被廣泛應用在各種醫療中。根據國際人道協會 ( HSI ) 報告,全球每年實驗動物使用量高達 1.15 億隻。即便臺灣的試驗研究機構積極推動減量,2020 年的使用量仍達 332 萬隻。
實驗動物的定義
何謂實驗動物?只要是被用於研究與教學、法定安全性測試 ( Biosafty testing ) ,或生產生物性製品 ( Bioproduct ) 的動物,皆屬於實驗動物。然而,一般在動物保護法律中,實驗動物通常更限縮於脊椎動物的範疇。在實驗室中,為研究疾病或特定生命現象,研究人員往往透過基因編輯或人為誘導,讓動物產生特定的病理變化,進而形成相應的動物模型,為疾病治療與藥物開發提供研究基礎。
實驗動物的爭議:道德與有效性的雙重挑戰
實驗動物的廣泛應用引發了兩方面的爭議:一是動物福利與道德考量,隨著動物權益意識提高,社會對動物在實驗中的待遇質疑增加,各國也相繼推出動物保護法規以減少動物使用和痛苦;二是實驗結果的有效性,由於動物與人類生理、代謝機制的差異,導致部分動物實驗結果難以在人體試驗中驗證。
基於以上考量,科學家和企業積極探索替代方案,如使用非哺乳類動物模型 ( 如斑馬魚、渦蟲 ) ,體外細胞培養,以及運用 AI 進行電腦模擬,以期提升實驗結果的人體相關性、降低對動物的依賴,並提高臨床轉譯效果。
類器官 / 器官晶片 ( Organoids / Organ-on-a-chip )
類器官的起源與發展
類器官的概念始於 1990 年代初期,初期因為細胞培養的技術與成本問題難以普及。直到 2009 年,荷蘭科學家 Hans Clevers 團隊成功在體外分化出腸道隱窩絨毛結構後,相關的培育研究才開始興盛。類器官是在實驗室中體外培養的 3D 立體細胞團,透過誘導性多功能幹細胞 ( iPSCs ) 或成體幹細胞 ( AdSCs ) 與細胞外基質 ( ECM ) 混合後,再輔以生長因子的引導,促進組織細胞往特定方向分化,模擬出人體器官的組織結構。然而,由於類器官的形狀與結構可能在不同實驗中產生異質性,標準化仍然是挑戰。
器官晶片技術的興起
2000 年微流體晶片技術的突破,促使「在晶片上培養組織」的概念誕生。器官晶片,也稱多通道 3D 微流體細胞培養晶片,是將所需求的細胞放入微系統晶片模型內培養,透過晶片上的通道來模擬器官內的細胞環境、血液與流體流動和化學信號,以重現器官內的動態活動與生理反應。由於晶片的透明性,也有助於實時追蹤觀察。2010 年起,Emulate, TissUse, CNBio, AxoSim 等知名廠商的加入,推動器官晶片進入快速成長階段。
應用與細胞來源
前述說明了細胞培養的過程與機制,接下來將聚焦於細胞的取得。目前,器官晶片的主要應用領域是藥物測試,尤其在癌症相關研究中廣泛使用。腫瘤細胞的提取方式包括傳統的腫瘤切片法,但在切除風險高的情況下,通常會採用其他非侵入性生物標記技術,例如目前廣泛應用的循環腫瘤細胞 ( CTC ) :當癌細胞發生轉移時,部分細胞會從腫瘤脫落並進入血液循環中,因此可以藉由細胞計數的蛋白質技術,以及 RT-PCR 測定 mRNA 的核酸技術,來識別循環腫瘤細胞。
器官晶片技術面臨的挑戰
儘管器官晶片在模擬人體生理上具有優勢,但仍面臨兩大挑戰:
- 規模化生產:目前,單一晶片所能測試的藥物數量有限,難以實現高通量測試,並且器官晶片的供應不足也導致生產成本高昂。因此,如何大規模生產並提高測試效率,是技術發展的關鍵。
- 多器官整合:在多器官、多晶片串聯上,模擬全身系統 ( 如血管、神經、內分泌 ) 的交互作用仍有技術難點,無法完整模擬人體或動物體的整體運作。因此,器官晶片目前仍無法完全取代動物實驗。
數位分身 ( Digital Twins )
數位分身的起源與應用
數位分身的概念最早由 Michael Grieves 博士提出,指的是在資訊平臺上模擬物理實體的狀態,由三個要素構成:現實中的實體物品、虛擬空間中的虛擬模型,以及連結兩者的數據與資訊。
這個概念廣泛應用在各個領域,而在生技醫療產業自然也衍生出相對應的使用場景。除了在製造端用於廠房設計,數位分身對替身醫療的最大貢獻在於輔助臨床決策。現階段實際投入使用,並通過美國食品和藥物管理局 ( FDA ) 核准的技術主要是電腦模擬測試 ( in silico ) :進行活體實驗前,先透過電腦模型模擬藥物篩檢與治療方案,以觀察藥物分子與細胞的相互作用。目前這類技術多針對特定的主題或部位,像是 Alya Red 的人體心臟建模。
數位分身的挑戰
醫療數位分身發展上的挑戰包含以下三項:
- 數據品質與精確性:構建電腦模擬模型需要大量且精準的數據,但數據的收集十分困難,且部分疾病的致病基因組未定序、病生理機轉不明,使得完整模擬人體變得困難。
- 模型開發與開源環境不足:現今尚未出現良好的模型開源環境,導致研究軟體的重複利用率低,增加實驗的時間和成本,使得開發進展緩慢。
- 數據整合與運算複雜度:模擬多器官及多時間尺度系統的數據整合不易,導致運算複雜度上升,降低模擬的精確度。
然而,隨著 AI 與機器學習 ( ML ) 的進步,異質數據的標準化處理及多維模型學習能力不斷提升。若能充分運用 AI 技術,逐步實現虛擬人類分身 ( Virtual Human Twin ) ,或能成為人工器官無法完整模擬人類整體運作的突破口。
案例:AI 加速替身醫療的實驗室流程
AI 在替身醫療領域的應用,不僅協助技術發展,也提升了實驗室的運作效率。臺灣替身醫療知名公司「精拓生技」便引入 AI,以實現實驗室工作流程的自動化,並應對實驗室操作標準化的挑戰。
傳統實驗室的檢驗流程常受操作人員技術、習慣,以及各實驗室內部操作常規的影響,導致步驟難以標準化,從而影響檢驗結果的一致性。而 AI 的引入能通過機器學習分析實驗數據,協助自動化處理數據收集和分析,減少人工干預,提升實驗效率和結果穩定性。
精拓生技的創辦人陳柏翰先生,具備資料工程師背景,他分享:「在訓練 AI 模型的過程中,我們遇到了許多意料之外的挑戰。」其中一個主要挑戰就是需要為實驗流程建立標準作業程序 ( SOP ),甚至連檢體的擺放方式都需標準化,以便 AI 進行分析。
此外,針對不同品牌的檢驗儀器之間的數據格式不一致的問題,陳先生進一步說明,某些儀器需要專用軟體來查看結果,或只能輸出特定格式的數據,甚至資料欄位也有所差異。要實現完全的自動化,必須確保這些不同儀器的數據格式能相互讀取或合併。因此,團隊需要額外處理這些數據格式,將其統一,或轉換為程式可以讀取的格式,從而順利進行 AI 的自動化分析流程。
EPA 動物實驗新政策擱置,醫療替代技術的下一步怎麼走?
近期,美國環保署 ( EPA ) 擱置了全面取代動物實驗的具體時間表,引起了廣泛關注。早在 2019 年,EPA 曾提出計劃在 2025 年前減少 30% 對哺乳類動物的實驗,並在 2035 年全面停止動物實驗。然而,2024 年初發布的相關文件中,這兩個具體期限卻不再被提及,業界不免擔心這是否會影響類器官、器官晶片,以及數位分身等技術的發展進程?
雖然政策和法規在一定程度上引導和限制技術的發展方向,但對企業而言,推動新技術的最大動力依然來自於潛在的獲利機會與市場需求。以體外模擬技術 ( 如類器官與器官晶片 ) 替代活體實驗,並輔助藥物開發,已被視為醫療產業的未來趨勢。對於企業而言,核心挑戰在於如何有效降低成本與風險,加速技術開發,並早日實現盈利目標。
為了達成這些目標,專注於發展替代方案的企業可以從以下幾方面入手:
- 選定具有潛力的適應症:鎖定可涵蓋廣泛客戶需求的適應症,能夠更好地實現產品市場契合度,並最大化商業化的成功機會。
- 吸引大型機構資金支持:大型機構和投資者的資金支援,對於技術開發初期的穩定推進至關重要。此外,與學術機構和政府單位合作,可能在研發與臨床應用方面獲得更多資源。
- 尋找教育成本低的市場進入點:優先選擇對新技術接受度高,且教育成本相對較低的市場,能夠加快產品推廣速度,減少市場切入的阻力。
- 結合 AI 技術:借助 AI 和大數據分析,能夠加速實驗模擬、藥物篩選以及技術開發流程,進一步縮短生產週期並降低研發成本。
透過這些策略,企業將能更有效的推動替代技術的發展,為整體醫療產業及病患帶來嶄新的未來,也為非動物實驗的推廣提供更具體可行的方向。

